![]()
| Summenformel: | Na2S2O3 x 5 H2O |
Molekülmasse: 248,2 g/mol
Vorschrift (nach Ph.Eur. 2. Ausg., Nachtrag 1999)
Benötigte Chemikalien:
| Natriumthiosulfat
Pentahydrat (Reinheit: zur Analyse oder Reagens Ph.Eur. NT99) |
| Natriumcarbonat
Decahydrat (Reinheit: zur Analyse oder Reagens Ph.Eur. NT99) |
| gereinigtes
Wasser (destilliert oder demineralisiert), kohlendioxidfrei Gereinigtes Wasser wird einige Minuten lang sprudelnd abgekocht und beim Abkühlen vor Luftzutritt geschützt (z.B. durch Abfüllen in eine Laborflasche aus Duranglas). |
Herstellung:
25 g (also wenig mehr als 0,1 mol) Natriumthiosulfat-5-hydrat ACS (Art. 1304) und 0,2 g Natriumcarbonat-10-hydrat (Art. 0403) werden eingewogen und in dem kohlendioxidfreiem Wasser zu 1000,0 ml gelöst.
Der Zusatz von etwas Natriumcarbonat soll die Beständigkeit der fertigen Maßlösung erhöhen. Um eine Zersetzung durch Kohlensäure zu vermeiden, wird zur Herstellung Wasser verwendet, das durch vorheriges Abkochen kohlendioxidfrei gemacht worden ist.
Einstellung
Benötigte Chemikalien und Maßlösungen:
| Kaliumiodid-Lösung
R (166 g/L KI) Herst.: 16,6 g Kaliumiodid zur Analyse oder reinst (Art. 0300) werden in Wasser zu 100 ml gelöst. |
Natriumthiosulfat-Maßlösung
0,1 M (hergestellt wie oben beschrieben) |
| Salzsäure
R1 (250 g/L HCl) Herst.: 70 ml konzentrierte Salzsäure ACS (Art. 0505) werden mit Wasser zu 100 ml verdünnt. |
gereinigtes Wasser (destilliert oder demineralisiert) |
| Kaliumbromat-Maßlösung
0,2 N = 1/30 M Herst.: 5,5670 g (0,0333 mol) Kaliumbromat ACS (Art. 7072) werden im Meßkolben mit Wasser zu 1000,0 ml gelöst. |
Stärkelösung
als Indikator Herst.: 1 g lösl. Stärke (Art. 0521) wird mit 5 ml Wasser angerieben und die Mischung unter Umrühren in siedendes Wasser gegeben. |
Vorgehensweise:
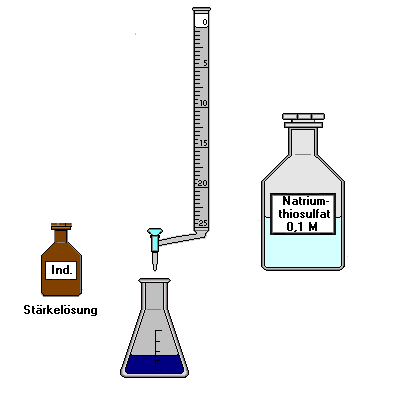
| Abb.
rechts: Vorbereitung zur Titration - Mit einer Vollpipette werden 10 ml
Kaliumbromat-Lösung 0,2 N (= 1/30 M) abgemessen, in das
Titrationsgefäß gebracht und (in dieser Reihenfolge) mit 40 ml gereinigtem Wasser, 10 ml
Kaliumiodid-Lösung und 5 ml Salzsäure versetzt. In der Lösung bildet sich durch
Oxidation von Iodidionen rotbraunes Iod. Das Bromat wird dabei zu Bromid reduziert nach: BrO3 - + 6 H+ + 6 e - ---> Br - + 3 H2O Steht Kaliumbromat-Lösung 0,1 N (= 1/60 M) zur Verfügung, so nimmt man davon 20 ml und entsprechend 10 ml weniger Wasser. |
|
 |
Das
ausgeschiedene Iod wird mit der einzustellenden Natriumthiosulfat-Maßlösung 0,1 M
titriert, wobei gegen Ende der Titration 1 ml Stärke-Lösung als Indikator zugegeben
wird. Näheres über diese Titration erfahren Sie im Artikel Gehaltsbestimmung von Kaliumpermanganat. |
| F (Natriumthiosulfat) = | F (Kaliumbromat) x 20/a |
wobei a = Verbrauch 0,1 N Natriumthiosulfatlösung (in Milliliter)
![]()
Erstellt am 28.09.1999 * Letzte Änderung am 28.09.1999 © OMIKRON GmbH