Riechstoff-Lexikon B
![]()
Benzylalkohol
|
Andere Namen: |
"Phenylmethanol", "Benzolmethanol"; lat.: Alcohol benzylicus; engl.: benzyl alcohol, benzenemethanol, phenylmethanol, phenylcarbinol, a-hydroxy-toluene; frz.: alcool benzylique; ital.: alcool benzilico |
|
CAS-Nr.: |
[100-51-6] |
|
EG-/EINECS-Nr.: |
202-859-9 |
|
Arctander: |
290 |
|
Fenaroli: |
45 |
|
FEMA-No.: |
2137 |
Molmasse Mr
/F.W. = 108,13 g/mol
Summenformel (Linienformel): C7H8O / C6H5CH2OH
Strukturformel:

Vorkommen:
Dieser Riech- und Aromastoff ist ein
natürlicher Bestandteil vieler ätherischer Blütenöle, insbesondere von
"gehaltvollen" Duftpflanzen wie Ylang-Ylang, Tuberose, Jasmin und
Goldlack. Auch in echtem Rosenöl, Hyazinthen- und Cassienblüten Absolues sowie
im Duft von Robinia pseudo-acacia
wurde Benzylalkohol aufgefunden. In Form des Benzoats und Cinnamats weiterhin
enthalten in verschiedenen aromatischen Balsamen (Perubalsam, Tolubalsam,
Styrax). Die industrielle Duftstoffherstellung erfolgt ausgehend von Toluol, da
die chemische Konstitution des Syntheseprodukts der natürlichen Struktur
entspricht und eine Isolierung aus pflanzlichen Ausgangsstoffen sehr teuer und
aufwendig wäre. Als realistische Möglichkeit, natürliche Quellen anzuzapfen,
wäre allenfalls die Reduktion der aus Benzoeharz
isolierten Benzoesäure zu nennen, jedoch hat diese Methode nie technische
Bedeutung erlangt.
Beschreibung
Benzylalkohol ist eine farblose, klare,
lichtbrechende und ölige Flüssigkeit, die in Wasser begrenzt löslich ist (100 g
Wasser nehmen ca. 4 g B. auf). Der Stoff ist mischbar mit Ethanol, Diethylether
und Chloroform sowie mit den meisten fetten und etherischen Ölen.
Duftcharakteristik / odor profile
Der Dufteindruck ist angenehm und etwas
süßlich, jedoch nicht sehr intensiv. Der Stoff besitzt ein schwaches
Mandelaroma, das sich bei Lagerung an der Luft verstärkt (Bildung von Benzaldehyd)
und einen scharfen, brennenden Geschmack.
engl.:
faintly aromatic, pleasant, slightly sweet, almond-like, with a sharp, burning
taste
Verwendung
Benzylalkohol ist durch Anlage 6 der
deutschen Kosmetikverordnung in einer Konzentration bis zu 1% (bezogen auf das
fertige Produkt) als Konservierungsstoff für kosmetische Mittel zugelassen. Die
Verträglichkeit ist in aller Regel gut, Hautirritationen sind - wie bei fast
allen Konservierungsstoffen - aber möglich. Im ÖKO-TEST Ratgeber Kosmetik beurteilt Dr. Dieter Wundram den Inhaltsstoff als
"empfehlenswert". Die (Lebensmittel-) Zusatzstoff-Zulassungsverordnung
läßt Benzylalkohol als Lösungsmittel
für Farbstoffe bestimmter Anwendungsgebiete (z.B. Ostereierfarben,
Käseüberzüge) zu.
In der Parfümerie und Aromenproduktion wird
der aromatische Alkohol aufgrund seines guten Lösungsvermögens und dem unaufdringlichen
Duft vorwiegend eingesetzt als Verdünnungs- und Lösungsmittel. In manchen
Blumenkompositionen zur Abrundung und als Fixateur.
Der Alkohol ist ein wichtiges
Ausgangsprodukt für Riechstoffsynthesen, vor allem zur Herstellung der
verschiedenen Benzylester (Benzylacetat, Benzylbenzoat, Benzylpropionat,
Benzylcinnamat usw.). Bisweilen auch für andere organische Synthesen eingesetzt.
Technisch verwendet als Bestandteil bzw.
Lösungsmittel von Lacken, Kunstharzen und Farbstoffen, als Textilhilfsmittel
und für Kohlepapiere. In der pharmazeutischen Industrie dient der Stoff als
Konservans, z.B. in parenteral verabreichten Arzneiformen. Benzylalkohol wirkt
auch lokalanaesthesierend.
Als Reagenz bei der Prüfung von Cyanocobalamin nach dem Europäischen
Arzneibuch 1975.
Darstellung
Der Stoff kann durch Umsetzung von
Benzylchlorid mit Alkalicarbonaten (bzw. Erdalkali-Hydroxiden) in der Wärme
oder durch Reduktion von Benzaldehyd erhalten werden. Setzt man z.B.
Benzaldehyd mit Formaldehyd um, so wirkt der Formaldehyd als
"Hydridionendonator"; dabei wird er zu Ameisensäure oxidiert (sog.
"gekreuzte" Cannizzaro-Reaktion):
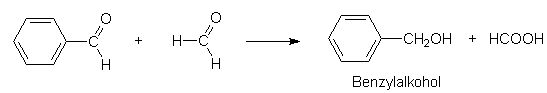
Die Reaktion wird basisch katalysiert
(Zusatz von Kalilauge); zu Mechanismus und Arbeitsvorschrift siehe Organikum, S. 533. Eine ähnliche
Arbeitsvorschrift findet man auch in Organic Syntheses, Coll. Vol. II., p. 591
(analog der Darstellung von p-Methylbenzylalkohol).
1 Mol Benzoesäure-ethylester liefert bei der
Reduktion mit 0,5 Mol Lithiumaluminiumhydrid in 90%iger Ausbeute Benzylalkohol
(Fieser/Fieser, S. 327):
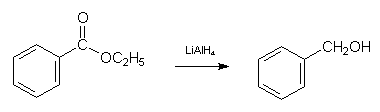
Bedeutsam ist auch die Möglichkeit, Toluol
mit Luftsauerstoff zu Benzylhydroperoxid zu oxidieren, welches bei der
Hydrolyse (neben etwas Benzaldehyd) Benzylalkohol liefert. Benzylalkohol, der
noch Reste von Benzaldehyd enthält, kann durch Kochen mit starker Natronlauge
benzaldehydfrei gemacht werden.
VERSUCH:
Man gibt zu einigen Tropfen Benzylalkohol
vorsichtig konzentrierte Schwefelsäure. Anstelle einer Esterbildung tritt unter
Wasserabspaltung Verharzung auf (Polymerisation). Ethanol würde - je nach
Reaktionsbedingungen - Ethylsulfat oder Diethylether liefern.
Chemische und physikalische
Kenndaten:
|
Parameter |
Wert (z.B. RK=Roth/Kormann, R=Römpp, B=Bauer et al.) |
Bereich (FCC 3) |
|
Dichte 20 °C / s.g. |
1,0419 (B);1,045 (R) |
1,042 - 1,047 (25 °C) |
|
Brechungsindex / refr.
index |
1,5396 (B, RK) |
1,539 - 1,541 |
|
Schmelzpunkt / mp |
-15 °C (RK) |
--- |
|
Siedepunkt / bp |
205 °C (Organikum); 205,4
°C (B, RK) |
206 °C (decomp.) |
|
Destillationsbereich /
dist. range |
--- |
NLT 95% between 202.5 and 206.5° |
|
Löslichkeit in Ethanol |
1:1,5 Vol. L50% (RK) |
miscible |
|
Löslichkeit in Wasser |
1 g in 25
g (RK); 1 ml in 30 ml vollständig und klar (Ph.Eur.) |
1 ml in 30 ml |
|
Grenzwert für Aldehyde /
aldehydes |
--- |
0,2% |
Vorschriften
Verordnung über brennbare Flüssigkeiten
(VbF): A II / Flammpunkt: 96 °C
Wassergefährdungsklasse (D): WGK 1
(schwach wassergefährdend)
Schweizer Giftklasse (CH): 4
![]()
Erstellt am 26.07.1999 * Letzte Änderung am
28.08.2013
Nachdruck nur mit ausdrücklicher Genehmigung
der © OMIKRON GmbH Naturwaren
[Literaturverzeichnis] * [Inhaltsverzeichnis]